一、背景介绍
开发先进的电解液是开发下一代锂离子电池(LIBs)不可或缺的重要组成部分。然而,Li+与各种溶剂之间的强溶剂化相互作用,往往导致Li+去溶剂缓慢和溶剂共嵌到石墨电极中,从而极大地限制了电解液设计。相比之下,非配位共溶剂(非溶剂)对Li+保持惰性,但由于较小的非溶剂-溶剂相互作用,将体相溶剂化网络分离为单个溶剂簇,为调整Li+-溶剂的强度和拓扑结构铺平了另一条途径。
此外,理想的非溶剂可以改善物理性能(如粘度、共晶溶剂和润湿性),并为电解液设计激发一个新的维度。因此,探索这些分子相互作用(如Li+-溶剂吸引和非溶剂-溶剂相互作用)和描述它们的临界条件对于开发多功能电解液和调整其电化学行为是势在必行的。
之前的研究中,华中科技大学谢佳教授和曾子琪博士等人(-90~90°C!非溶剂化相互作用实现宽温域PC基电解液)在Adv.Energy Mater.上以“RejuvenatingPropylene Carbonate-based Electrolyte Through NonsolvatingInteractions for Wide-Temperature Li-ionsBatteries”为题提出了通过在PC和锂盐构成的PC基电解液中加入氟苯(FB),基于非溶剂化的相互作用来调节Li+-PC的强度和拓扑结构,使得PC溶剂宽的温度范围(-90~90°C)内实现石墨负极锂离子全电池的循环。
作者认为,在2.3M的较低锂盐浓度下,FB能够削弱PC和Li+之间的亲和力,而溶剂化结构没有显著变化,电化学稳定性增强,且高低温电化学性能明显提高。
针对DME、DMSO、TMP、PC和DEC等一类具有强溶剂化效应的溶剂,本文提出的非溶剂化相互作用来调节Li+的溶剂化结构是否也适用于此呢?
二、正文部分
01 成果简介
在此,华中科技大学谢佳教授和曾子琪博士等人提出了偶极-偶极相互作用的机制,通过调节Li+、溶剂和非配位分子(非溶剂)之间的相互作用来促进Li+去溶剂和抑制溶剂化Li+共嵌。
具体而言,在中等锂盐浓度下,非溶剂抵消静电吸引,以抑制Li+和溶剂之间的亲和力,而不改变初级溶剂化结构。因此,Li+溶剂化强度减弱,使去溶剂化变得容易,从而与石墨负极在各种溶剂中具有优异的电化学相容性,包括DME(乙二醇二甲醚)、DMSO(二甲基亚砜)、TMP(磷酸三甲酯)、PC(碳酸丙烯酯)和DEC(碳酸二乙酯)。
因此,本文提出的偶极子-偶极子相互作用的策略可以将电解液设计的视野扩展到先进的LIBs中。该研究以题目为“Dipole-dipoleInteractions for Inhibiting Solvent Co-intercalation into GraphiteAnode to Extend the Horizon of ElectrolyteDesign”的论文发表在材料领域国际顶级期刊《EnergyEnviron. Sci.》。
02 研究亮点
1.本文提出了一个分子相互作用模型来调节溶剂化Li+的界面行为,非溶剂远离了Li+的溶剂化壳层,同时对极性溶剂产生了相当大的偶极-偶极相互作用,削弱了Li+与溶剂之间的库仑吸引力;
2.松散的Li+-溶剂团簇在热力学上有利于有效的去溶剂化,从而降低了去溶剂化势垒,改善了电化学稳定性
3.在中等锂盐浓度(临界边界条件)下,利用各种非溶剂(FB、ClB、BrB和CB),基于其他正极不稳定溶剂(如DME、DMSO、TMP、PC和DEC)验证了该模型。
03 图文导读
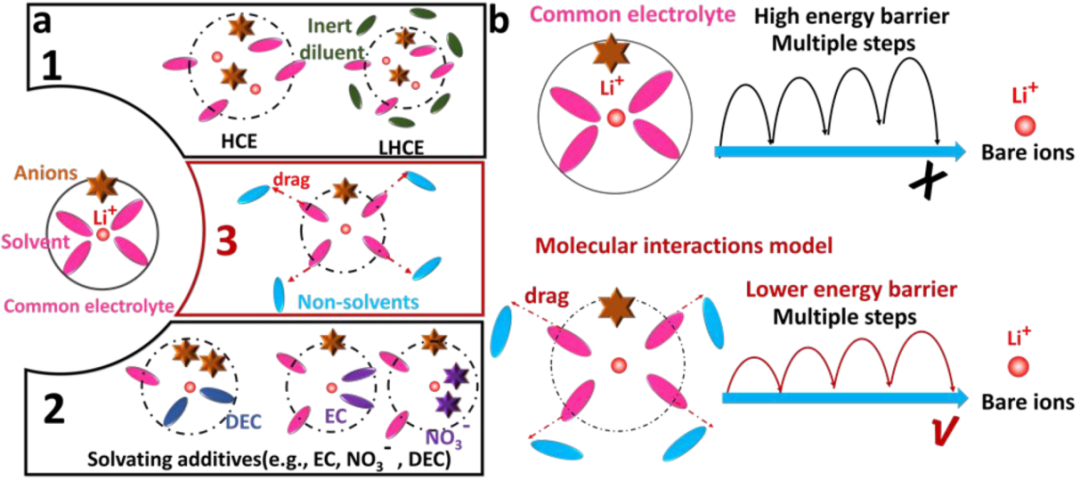
【方案1】已建立的溶剂化结构及去脱溶剂过程的示意图。(a-1)高浓度电解液和局部高浓度电解液的溶剂化化学性质;(a-2)具有不同溶剂化组分(如EC、LiNO3和DEC)的电解液的溶剂化化学性质;(a-3)加入非溶剂后的电解液的溶剂化化学性质和分子相互作用模型;(b)普通电解液和非溶剂改性电解液的其去溶剂化机理。
1.电解液成分的合理设计
在低浓度摩尔比(LiFSI/DME<1:4)时,石墨//Li电池表现出可逆共嵌;当LiFSI/DME=1:3(LiFSI-3DME)时,可以获得更高的220mAh g-1可逆容量(图1a)。相比之下,LiFSI-2DME粘度的急剧增加,表现出高极化和低容量。值得注意的是,LiFSI/DMEMRs的增加在一定程度上抑制了Li+-DME共嵌,但仍存在高粘度、低电导率和残留共嵌(0.8V平台)。
在LiFSI-3DME体系中引入氟苯(FB),共嵌被完全抑制,石墨的理论容量高达372mAhg-1,初始库仑效率高达86%(图1b)。此外,这种电解液(LiFSI-3DME-7FB)在石墨//Li电池中显示出超过200次循环的稳定循环,容量保持率高达94%(图1c)。
OperandoXRD显示LiFSI-3DME电解液中显示出明显的(002)峰分裂(图1d)。相比之下,在FB支持的DME电解液中,石墨在0.3V以上保持(002)峰,表明在Li+嵌入之前,抑制了Li+-DME共嵌和稳定了层状结构。CV结果进一步验证了引入FB后DME基电解液相容性的改善(图1e)。
值得注意的是,不同于常见的HCEs和LHCEs,应该开发一种新的模型来解释仅包含锂盐、溶剂和FB的电解液设计中存在的抑制共嵌行为。
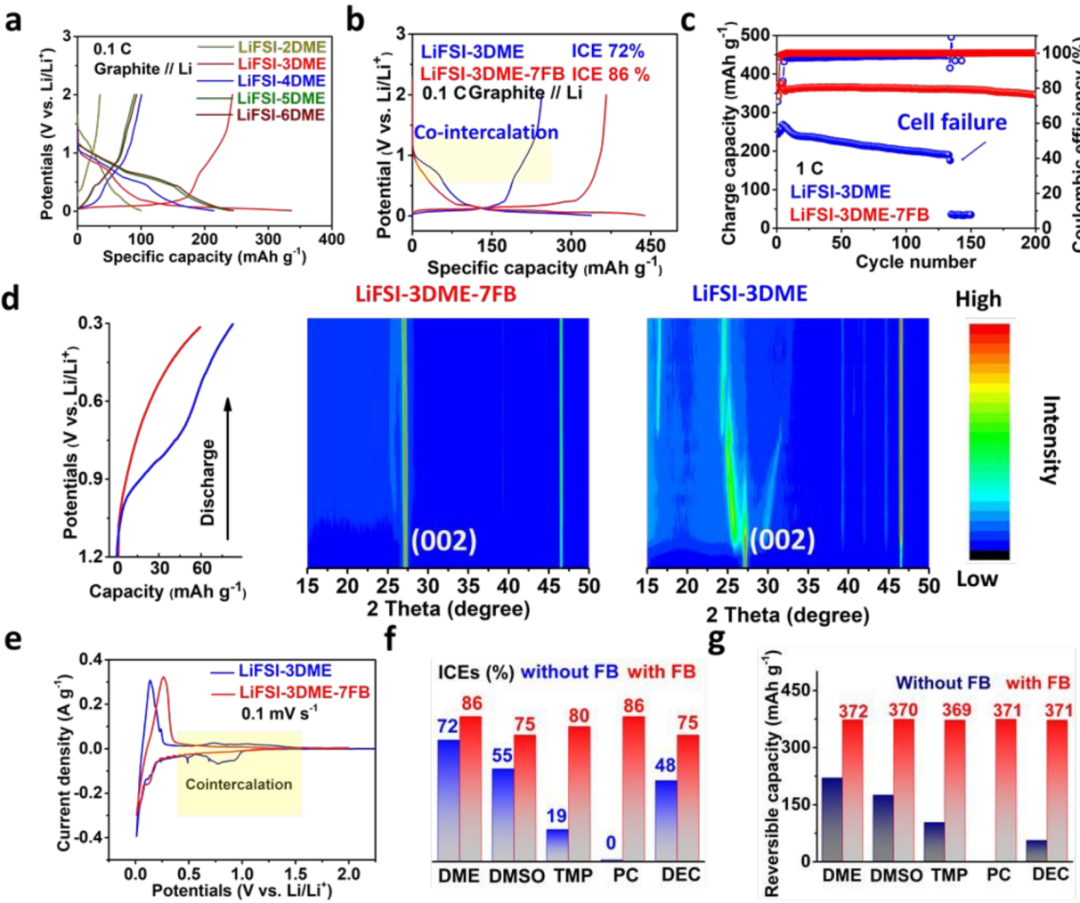
【图1】溶剂共嵌表征。(a,b)不同电解液中石墨/Li电池的充放电曲线;(c)石墨/Li电池的循环稳定性;(d)原位XRD表征;(e)LiFSI-3DME和LiFSI-3DME-7FB电解液中石墨/Li电池的CV曲线;(e,f)加入FB后ICEs和可逆容量的比较。
2.模型通用性演示和溶剂到非溶剂的选择
为了揭示电解液的设计和建立分子相互作用模型,本文系统地研究了DMSO、TMP、PC和DEC在石墨//Li电池中的阴极稳定性。值得注意的是,石墨在低浓度下存在严重的共嵌,但随着锂盐/溶剂MRs的增加,相容性逐渐增强。因此,根据放电曲线,LiFSI-3DMSO(4.7M)、LiFSI-3TMP(3.1M)、LiFSI-5PC(2.3M)和LiFSI-6MEC(1.4M)为临界摩尔比,高MRs下可逆循环,低MRs下电解液失效。
当FB加入后,电化学可逆性行为,ICEs分别增强为75%、80%、86%和75%。此外,在石墨相容溶剂(如EMC、DMC和EC)中也研究了FB的效应,与原始电解液相比,其倍率性能大大提高。
同时,考虑到FB的脱氟可能促进初始循环过程中石墨表面含LiF的SEI的形成,作者使用其他无F原子的非溶剂(如ClB、BrB和CH)取代FB。含ClB和BrB的电解液的电化学相容性和可逆性显著增强,其高ICEs分别为85.9%和86.6%(图2a,b)。更重要的是,仅含C和H原子的环己烷(CH)在LiFSI-5PC-7CH中也显示了石墨的可逆循环(图2c)。
以上结果表明,非溶剂并不局限于FB,还可以扩展到其他非溶剂,如ClB、BrB和CH(图2d),证明了该设计原理的通用性。此外,含FB的电解液保证了在SEI较差的情况下石墨的正常运行,进一步说明了电解液结构和偶极-偶极相互作用的主导作用。
此外,其他报道也揭示了SEI对抑制溶剂共插层的有限作用,突出了体相电解液设计的意义。这些结果表明:(i)非溶剂的影响不是由其成膜能力引起的;(ii)体相电解液或Li+-溶剂配位可能比SEI对抑制Li+-溶剂共嵌的作用更大。
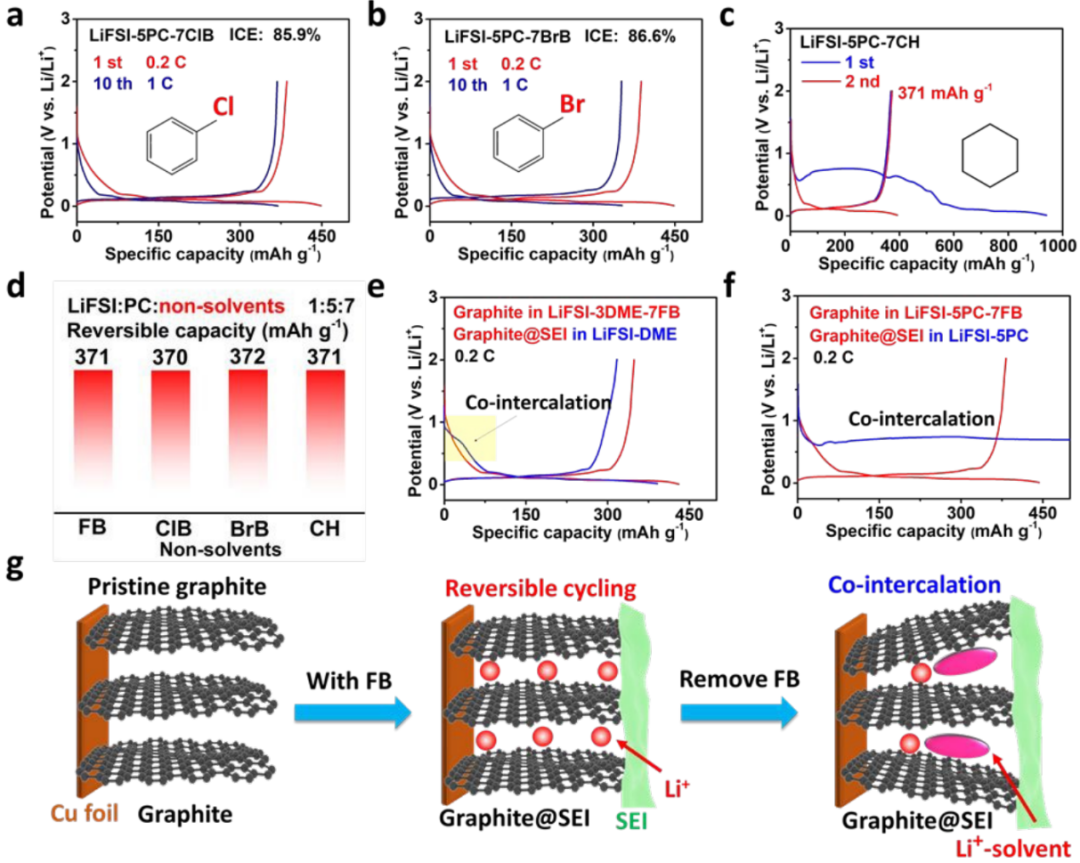
【图2】SEI非溶剂的选择及抑制共嵌的效果验证。(a-c)Li-FiSI-5PC-7ClB、LiFSI-5PC-7BrB和LiFSI-5PC-7CH中石墨/Li电池的充放电曲线;(d)加入不同非溶剂后的可逆容量;(e,f)SEI涂层石墨在无FB的电解液中重新组装;(g)含FB和无FB的电解液中石墨电极的原理图。
3. 分子相互作用和溶剂化结构
为了确定与石墨的相容性增强的关键因素,利用核磁共振(NMR)和拉曼分析研究了锂盐、溶剂和非溶剂的相互作用。与FB混合后,DME中1H核的信号从3.97ppm转移到3.41ppm,与FB中1H核从6.90ppm下降到7.12ppm完全一致,表明FB与DME之间存在分子相互作用(图3a)。
在DME中LiFSI解离后,DME的1H信号从3.97ppm移动到3.78ppm,表明DME和Li+之间具有很强的库仑吸引力(图3b)。将FB引入到LiFSI-3DME电解液中,由于Li+-DME与FB-DME之间的累积相互作用,导致DME中1H核的进一步上升(图3c)。
结果表明,分子尺度竞争模型显示Li+-DME团簇具有较强的库仑吸引力,而FB-DME具有相对较弱的相互作用(偶极-偶极相互作用)。此外,在与PC、DMSO和TMP的电解质中也观察到类似的分子相互作用,表明在体相电解液中普遍存在分子规模的竞争。
同时,通过拉曼数据揭示了溶剂化结构,CIPs和AGGs的增加(从46%增加到53%)不足以形成阴离子衍生的SEI,而通过重新组装SEI涂层石墨显示,SEI对抑制共嵌的作用有限(图2e-g)。
FB与DME之间的偶极-偶极相互作用明显弱于Li+与DME之间的库仑吸引,导致Li+-DME强度降低,但保留了溶剂化结构,如MDinterwetten与威廉的赔率体系
所示(图3f)。基于以上讨论,LiFSI-3DME和LiFSI-3DME-7FB的溶剂化结构,在前者中,极性溶剂(如DME和PC)与Li+之间的高亲和力有助于产生较强的库仑吸引力,导致了稳定和紧凑的溶剂化结构(图3g)。
当引入FB时,FB和DME之间的偶极-偶极相互作用部分削弱了Li+-DME的吸引力,构建了一个相对松散的溶剂化结构,而没有明显排挤DME分子(图3h)。
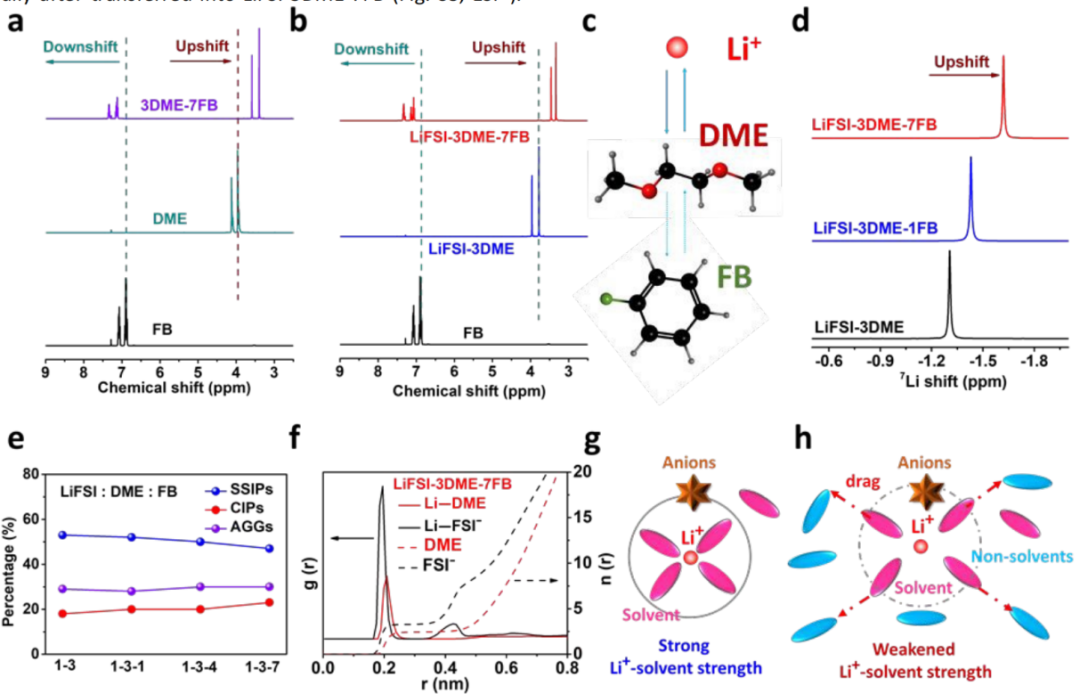
【图3】非配位的相互作用和溶剂化结构。(a)FB、DME和混合溶液的1H信号;(b)FB、LiFSI-3DME和LiFSI-3DME-7FB信号;(c)FB、PC和Li+之间的相互作用;(d)各种电解液的7Li信号;(e,f)添加FB后的SSIPs、CIPs和AGGs的百分比,以及游离DME和Li+-DME的百分比;(g,h)LiFSI-3DME和LiFSI-3DME-7FB的溶剂化结构示意图。
4.去溶剂化和界面行为
实验表明,去溶剂化作用主要在电极/电解液界面上进行,并决定了电化学行为。FB降低了DME基电解液中-3.44到-1.23eV的结合能,以及PC基电解液中-2.73到-0.71eV的结合能,表明Li+-溶剂化能力的减弱(图4a)。同时,还计算了均方位移(MSD)随时间的变化,以了解相对松散的溶剂化壳层和相对降低的Li+-DME强度。加入FB后,Li+的扩散系数从7.87×10-9增加到
相比之下,原始电解液(如LiFSI-3DME、LiFSI-5PC)具有强结合和紧密的配合,具有缓慢的去溶剂化和共嵌发生(图4d)。此外,FB、PC和DME在石墨(001)平面上的吸附能分别为-0.513、-0.464和-0.817eV,FB的吸收能力强于PC,但略低于DME。然而,LiFSI-3DME-7FB中较高的FB含量补偿了这种吸收能隙,使得FB在石墨表面的积累(图4e)。加入FB后,石墨表面附近DME的DME频率明显降低,导致DME还原的可能性较小(图4f,g)这些结果表明,FB削弱了Li+-溶剂的吸引力,保护了溶剂在石墨表面附近的电子交换,从而增加了电化学相容性,添加FB也降低了粘度,增加了润湿性。
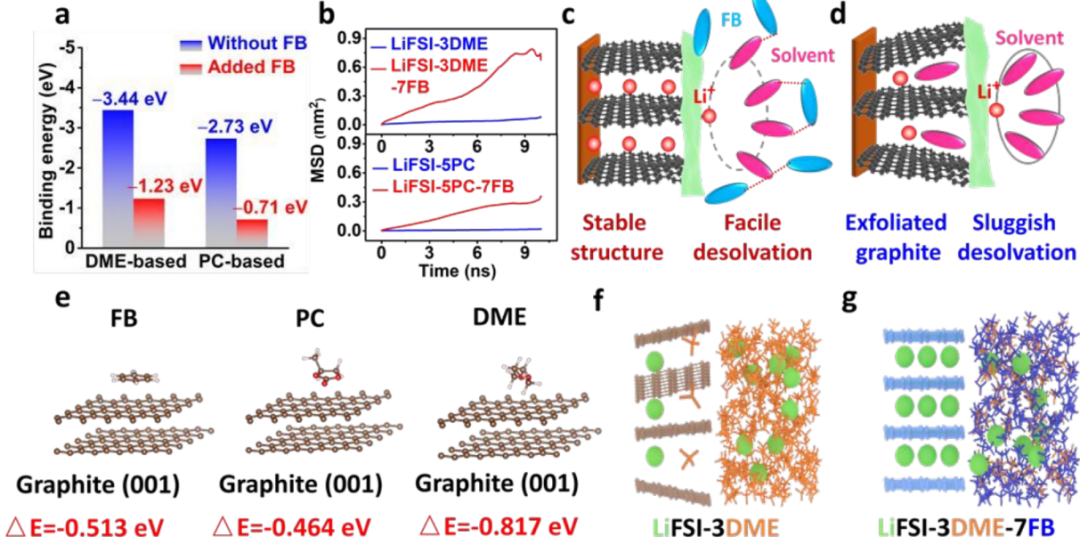
【图4】添加FB后的去溶剂化和界面机理。(a)加入FB前后Li+-溶剂的结合能;(b)MSD在DME和PC电解液中与时间的函数;(c,d)LiFSI-3DME-7FB和LiFSI-3DME在石墨表面去溶剂的插图;(e)FB、PC和DME在石墨(001)平面上的吸附能;(f,g)LiFSI-3DME和LiFSI-3DME-7FB中的界面状态示意图。
5.分子相互作用模型和关键因素
基于以上讨论,建立了分子相互作用模型来解释锂盐/溶剂/非溶剂的界面行为和临界MRs,该模型的本质在于Li+-溶剂(受锂盐浓度和溶剂类型的影响)和非溶剂-溶剂相互作用(受极性和非溶剂含量的影响)(图5a)。竞争力决定了去溶剂的能力,从而影响了电化学性能。强大的Li+-溶剂吸引力需要更强的非溶剂-溶剂相互作用来抵消和提供可行的去溶剂化,反之亦然。
结果表明,LiFSI-4DME-7FB和LiFSI-6PC-7FB不能在石墨//Li电池中发挥作用,在较低的锂盐/溶剂中,溶剂化壳层内主要的Li+溶剂团簇很难被偶极-偶极相互作用削弱(图5b)。此外,临界Li盐/溶剂MRs依赖于Li+-溶剂的结合能(溶剂类型),由于螯合作用,DME表现出的结合强度最强,其次是PC和DEC(图5c,d)。
具有最高结合能的Li+-DME团簇更难被分子相互作用所取代,需要更高的Li盐/溶剂的临界MRs(LiFSI-3DME)来降低Li+-DME的强度(图5b)。相比之下,PC和DEC可以在相对较低的Li盐/溶剂的临界MRs下工作。简而言之,锂盐/溶剂的临界MRs依赖于溶剂,并影响Li+-溶剂的相互作用。
对于偶极-偶极相互作用,含量和极性是两个关键因素。随着DME和PC中FB含量的增加,ICEs含量越高(图5e)。此外,对选定的非溶剂的电子云模拟中,CH具有对称的环状结构,呈现出平均分布的电子云。相比之下,由于卤素元素电负性较高的BrB,FB、和ClB分别在F、Cl和Br原子周围存在电子云堆积,可以合理地推测BrB-溶剂对的相互作用最强,因此提高石墨相容性所需的非溶剂含量最低(图5g)。
结果证实,建立非溶剂的有效值为LiFSI-5PC-1BrB、LiFSI-5PC-4ClB和LiFSI-5PC-7FB,与非溶剂的极性一致(图5f)。然而,环己烷具有最小的极性,即使在LiFSI-5PC-7CH的初始阶段也提供了最低的库仑效率,但仍能保持可逆循环(图2c)。
因此,Li+-溶剂和溶剂-非溶剂之间的微妙平衡可以通过这些途径来调整:1)根据溶剂的溶剂化能力调整锂盐/溶剂的摩尔比;2)利用高度极化的分子来增强偶极-偶极相互作用;3)在合理的范围内增加非溶剂的含量,以加强偶极-偶极相互作用。
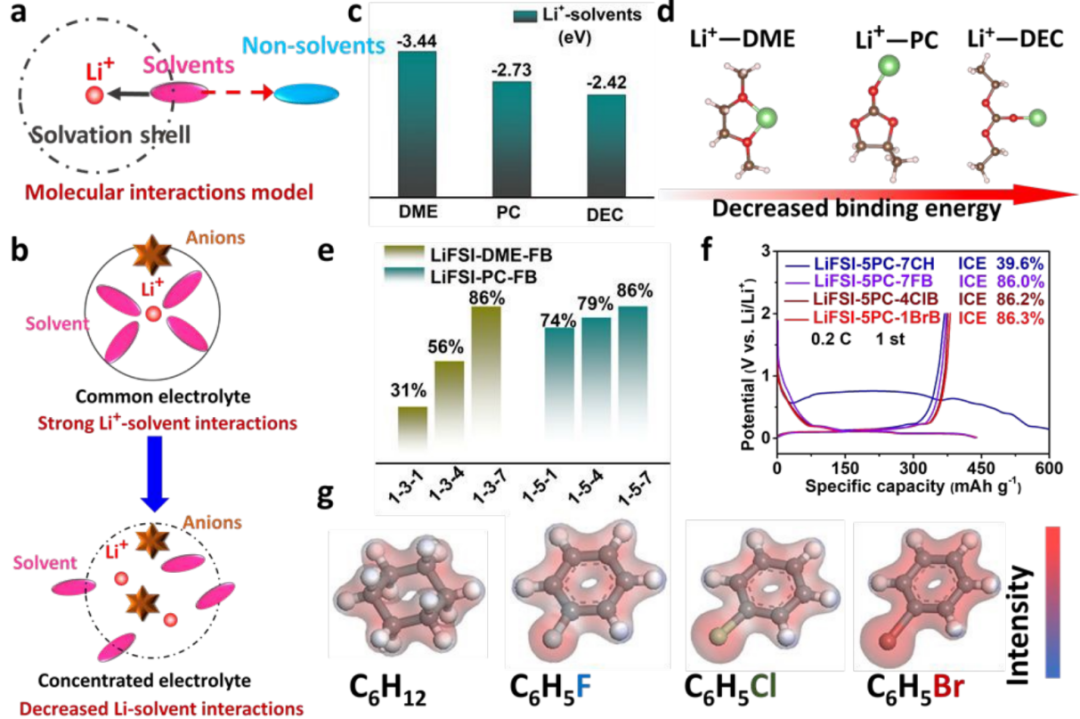
【图5】分子相互作用的模型和机制。(a)分子相互作用模型的示意图;(b)增加锂盐/溶剂MRs后,Li+-溶剂相互作用降低;(c)计算得到的Li+-溶剂结合能;(d)DME与PC和DEC的结合强度降低;(e)随着FB含量的增加,ICEs增加;(f)获得理想的ICEs所需的非溶剂含量;(g)不同非溶剂的模拟电子云。
6.所设计的电解液的性能指标和实用性
本文选择LiFSI-3DME-7FB和LiFSI-5PC-7FB作为原型,以证明这种分子相互作用模型在电解液中的实用性。结果表明,对于基于DME(LiFSI-3DME-7FB)和基于PC(LiFSI-5PC-7FB)的电解液的离子电导率均有所提高(图6a),其电解液的电化学窗口提升明显(图6b)。
因此,在锂盐、溶剂和非溶剂的合理配方下,电解液可以表现出多功能性能(如低温适应性、高导电性、高压耐受性)。此外,LiFePO4//石墨软包电池在LiFSI-3DME-7FB中可提供可逆的充电放电,其ICE高达92%(图6c)。最重要的是,PC基电解液在1.6AhLiFePO4//石墨软包电池中被评估,获得了91%的高ICE(图6d),表明在FB的协助下,其对LiFePO4和石墨都具有良好的相容性。
此外,软包电池可以在0.5C可逆循环160次循环,容量衰减小,表明PC基电解液在实际条件下的可靠性。
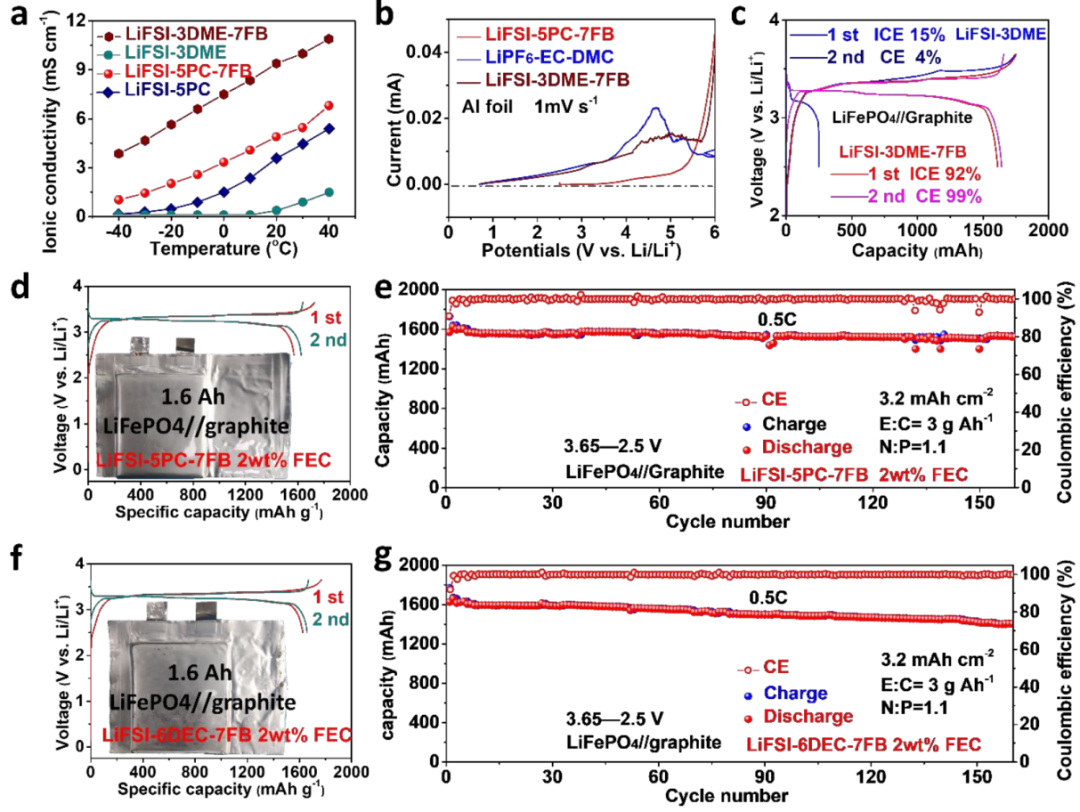
【图6】电解液的特征和应用。(a)PC基和DME基电解液在宽温范围内的电导率;(b)LSV测试结果;(c)DME基电解液中LiFePO4/石墨软包电池的充放电曲线;(d,e)LiFePO4//石墨软包电池在LiFSI-5PC-7FB电解液中的初始充放电曲线和循环稳定性;(f)LiFePO4//石墨软包电池在LiFSI-6DEC-7FB电解液中的初始充放电曲线和循环稳定性。
4、总结和展望
综上所述,本文提出了偶极-偶极相互作用模型,用于增强各种电解液与石墨负极的相容性,抑制了Li+-溶剂共嵌,保证了石墨晶格和增强了电化学可逆性。在该模型中,将非溶剂(如CH、FB、ClB和BrB)以临界锂盐/溶剂摩尔比引入溶剂(如DME、PC、DEC、TMP、DMSO)中,使Li+与溶剂的亲和力减弱,表面去溶剂和石墨相容性增强,而不改变初级溶剂化结构。该模型的本质取决于Li+溶剂与非溶剂的相互作用,两者决定了去溶剂动力学并决定了电化学行为。分子相互作用模型为提高中等锂盐浓度下多功能电解液与石墨负极的界面稳定性提供了一种新的策略,为优越的锂离子体相电解液设计提供了思路。
审核编辑:刘清
 电子发烧友App
电子发烧友App





























评论